- AVANT-PROPOS
- A la UNE
- PRESENTATION
- ACTUALITE SCIENTIFIQUE et TECHNOLOGIQUE
- ACTUALITE ARTISTIQUE
- BLOG
- CONSCIENCE
- PLANETE VIVANTE
- SCIENCES
- Sciences et histoire
- Science et politique
- Science/conscience
- Médecine de demain
- Le COVID-19
- COVID-19 - Journal d'une pandémie - 1 -
- COVID-19 - Journal d'une pandémie - 2 -
- COVID-19 - Journal d'une pandémie - 3 -
- COVID-19 - Journal d'une pandémie - 4 -
- COVID-19 - Journal d'une pandémie - 5 -
- COVID-19 - Journal d'une pandémie -6 -
- COVID-19 - Journal d'une pandémie - 7
- COVID-19 - Journal d'une pandémie - 8
- COVID -19 - Journal d'une pandémie - 9
- COVID-19 - Journal d'une pandémie - 10
- COVID-19 - Journal d'une pandemie - 11
- Arts et sciences
- L'homme debout
- Les débuts de la sagesse
- L'épopée scientifique
- Chimie, vivant... une si longue histoire !
- Introduction : 52 choses que je sais d'elle
- Sommaire
- 1 - Premiers pas
- I - A l'origine
- II - De la tetrasomia et l'alchimie à la chimie moderne
- III - al-kimiya
- IV - Alchimie : de l'aube à la fin de la Renaissance
- V - De l'(al)chimie à la chimie : une question de méthode ?
- VI - L'alchimie selon Newton, première partie
- VII - L'alchimie selon Newton, deuxième partie
- 2 - La chimie des Lumières
- XI - Chimie au siècle des Lumières - Introduction
- XII - Chimie au siècle des Lumières- Les affinités électives
- XIII - Diderot et la chimie
- XIV - Diderot - La chimie, pourquoi ?
- XV- Diderot chimiste
- XVI- La chimie et le Rêve de D'Alembert
- 3 - La chimie du vivant
- X - Chimie et Vivant - Introduction
- XIX - La génération spontanée
- XX - Fermentation : duel à 3 !
- XXI - Stéréochimie : clé du Vivant
- XXII - Homochiralité et origine de la vie
- XXIIc - Origine de la vie : état des lieux... provisoire
- XXIIb - Des biopolymères aux premiers organismes vivants
- XXIII- Stéréochimie et activité biologique
- XXIV - Chimie du cerveau - 1- Un cerveau, trois cerveaux, des cerveaux...
- XXV - Chimie du cerveau - 2 - Les neurotransmetteurs, messagers chimiques
- XXVI- Chimie du cerveau -3- Rôle des différents neurotransmetteurs
- XXXIV - Odorat, Odeurs et parfums
- XXXV- Bonnes et mauvaises odeurs
- XXXVI - Chimie et parfums
- XLIII - Chimie et couleur -1- De colore
- XLIV - Chimie et couleur -2- Couleurs végétales
- XLV - Chimie et couleur -3- : chimiothérapie et colorants
- XL- a - ADN, ARN, protéines
- XL- b - Chimie supramoléculaire
- XXXIX- Chimie et Synthetic Biology
- XLVI - Du génome au protéome
- 4 - Chimie et médecine
- VIII - Chimie et médecine : d'Hippocrate à Néron
- IX - Chimie et opium : voyages, voyages !
- XVII- Médecine et Chimie à Montpellier avant la Révolution
- XVIII - Le vitalisme de l'Ecole de Montpellier
- XXIX - Le médicament aujourd'hui
- XXVII - Autour de la sérotonine
- XXVIII - L'ocytocine
- XXX - Chimie, médecine, nanotechnologies
- L - Chimie et dopage -1- La chimie au service du dopage
- LI - Chimie et dopage - 2 - Les outils du chimiste contre le dopage
- XLIX - Image magnétique - 3 - de l'IRM au patient numérique
- 5 - La chimie moderne et ses hommes
- XXXI - Mendeleïev : un tableau de maître !
- XXXII - Mendeleïev : -2- Un chimiste russe au XIXème siècle
- XXXIII - Mendeleïev -3- Le fin mot de l'histoire
- XLI - Paul Sabatier, chimiste languedocien, prix Nobel 1912
- XLII - Victor Grignard, prix Nobel 1912
- XLVII - Image magnétique - 1 - Une histoire de spin
- XLVIII - Image magnétique - 2 - Mais que vient faire le chimiste dans cette galère ?
- 6 - Chimie : bonnes et mauvaises pratiques
- XXXVII- Du mauvais usage de la chimie
- XXXVIII- La chimie passe au vert
- Pour conclure
- Postface - Nylon by DuPont de Nemours
- Nylon... - Part A
- Nylon... - Part B
- Nylon... - Part C
- Nylon... - Part D
- La beauté des mathématiques
- Les sciences vers La Science
- La révolution numérique
- CRISPR-Cas9 : l'édition de gènes
- L'ombre de Frankenstein
- VOIR
- RECHERCHE, CONTACT
La ruée vers l'or

L'irruption des nanotechnologies dans le domaine de la biologie et de la médecine est un événement majeur dans le domaine thérapeutique et diagnostique. En particulier l'utilisation de nanoparticules s'est révélée particulièrement prometteuse comme méthode de vectorisation et technique d'imagerie.
La vectorisation
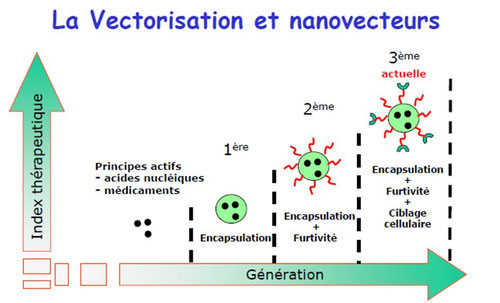
La vectorisation est un procédé thérapeutique qui consiste à administrer le médicament directement au niveau de la cellule malade afin d’éviter les sérieux effets secondaires que l'on observe par exemple dans les chimiothérapies anticancer. De ce fait, la dose administrée est significativement abaissée.
Le vecteur est l’élément transportant la molécule médicamenteuse. Son rôle est de protéger la molécule active des dégradations provoquées par les anticorps humains et de cibler l’endroit où cette molécule ira se fixer.
J'ai parlé ICI de Patrick Couvreur (chaire au Collège de France), un pionnier dans le domaine de la vectorisation et des nanomédicaments, qui a été le premier à montrer qu’il était possible d’utiliser des capsules submicroscopiques, d’une centaine de nanomètres, pour promouvoir la pénétration intracellulaire d'agents thérapeutiques.
L’adressage de molécules à visées thérapeutiques, constitue un défi majeur pour le traitement de nombre de pathologies, infectieuses, cancéreuses ou d’origine génétique.
En effet, de nombreuses molécules actives présentent des caractéristiques physicochimiques peu favorables au franchissement des barrières biologiques qui séparent le site d’administration du médicament de son site d’action. Ces molécules se heurtent souvent aux barrières enzymatiques qui provoquent leur dégradation et métabolisation rapides.
L’obtention de concentrations efficaces au niveau du site d’action ne peut donc se faire qu’avec une importante déperdition du principe actif (souvent plus de 90%) vers d’autres tissus ou cellules, ce qui occasionne des effets toxiques importants et parfois rédhibitoires (cas des agents anticancéreux).
Le développement de nanotechnologies dans le domaine des vecteurs de médicaments a donc pris un essor considérable au cours des dernières années.
Les progrès réalisés dans le domaine de la conception des matériaux permettent de préparer des nanosystèmes capables de libérer le principe actif en réponse à un stimulus externe : modification du pH, variation de température ou application d’un champ magnétique externe.
L'imagerie
D'un autre côté, il est également possible de concevoir des nanomédicaments dotés d’une double fonctionnalité : thérapeutique et diagnostique (imagerie), en rajoutant au sein du nanovecteur un agent d’imagerie (gadolinium, particules ultra-fines d’oxyde de fer, émulsions fluorés etc.)...
L'imagerie moléculaire permet, sur les organismes vivants, de visualiser les molécules présentes à l’intérieur des cellules ainsi que leur rôle dans le fonctionnement cellulaire, jusqu’au niveau du génome.
En cancérologie, elle permet non seulement d’établir des diagnostics de plus en plus précis et précoces, mais également de mesurer en temps réel l’efficacité des traitements administrés. Et c’est précisément l’évaluation de l’action des médicaments in vivo qui est la clé du développement de thérapies ciblées et personnalisées des cancers.
L'utilisation de l'IRM, technique non irradiante, peut permettre de combiner les avantages de l'imagerie moléculaire et l'excellente résolution spatiale et temporelle caractérisant cette méthode d'investigation. Le manque de sensibilité de la résonance magnétique peut être contournée par l'utilisation d'agents de contraste nanoparticulaires qui permettent de concentrer localement le contrastophore et de le lier à un biovecteur, ligand de la molécule cible.
L’IRM est particulièrement utile pour l’imagerie de l’angiogénèse tumorale. L’agent de ciblage angiogénique qui va permettre de diriger le vecteur jusqu’à la zone tumorale est généralement la séquence peptidique RGD( Arg–Gly–Asp, cible les récepteurs intégrines).
L’IRM a ainsi permis à maintes reprises d’imager la vascularisation tumorale, notamment à l’aide de nanoparticules offrant un signal amplifié. De nombreuses études ont employé des nanoparticules paramagnétiques pour suivre l’angiogenèse en ciblant les intégrines. Ainsi, des liposomes, chélatant du gadolinium (Gd3+), ont été couplés à un anticorps monoclonal des intégrines.
VOIR SUR LE SITE : De l'IRM au patient numérique
Les nanoparticules d'or
L'or "nanométrique" n'est pas de couleur or, mais rouge cramoisi ou bleu clair (selon la taille et la forme des particules).
Coupe de Lycurgue
Cette Coupe romaine (dite Coupe de Lycurgue) en verre, datée du 4e siècle après JC, est conservée au British Museum. Sa réputation est due à une caractéristique inhabituelle. A la lumière du jour (lumière réfléchie) elle paraît verte, mais si on place une source de lumière derrière la coupe, elle semble rouge (lumière transmise). Les verres romains présentant cette particularité sont très rares. Les analyses ont montré la présence dans le verre de nanoparticules métalliques (alliage d'or et d'argent) d'environ 70 nm.


Pourquoi les nanoparticules d'or ?
On sait que l'or métallique est caractérisé par une grande inertie chimique. Mais s’il est inerte à l'échelle macroscopique, l’or peut devenir extrêmement réactif sous la forme de particules nanométriques.
En effet à l’échelle nanométrique, plus nombreux en proportion et moins liés aux autres que dans un objet de taille supérieure, les atomes présents à la surface confèrent aux nanoparticules une grande réactivité chimique.
La production des nanoparticules d'or et des anticorps génère peu de déchets. C'est une alternative écologique à d'autres traitements plus polluants.
De plus, ces techniques sont moins onéreuses que les chimiothérapies classiques, car si l'or est un métal précieux, les quantités utilisées sont infimes.
L'or est préféré à d'autres métaux pour plusieurs raisons :
- sa biocompatibilité : l'or reste insensible aux dégradations potentielles in vivo,
- le fait que l'on puisse aisément fixer à sa surface des protéines anticorps ou antigènes.
Dès 2002, P. Couvreur décrivait des nanoparticules d'or composées d’un assemblage hybride organique/inorganique :
- avec une partie organique constituée de molécules d’acide folique (vitamine B9) capables de créer des liaisons covalentes avec d’autres cellules, par exemples de type ovariennes, colorectales, épithéliales ou mammaires.
- des particules d’or d'un diamètre pouvant varier de 5 à 20 nm.
Le lien entre les deux types de composants constituant la nanoparticule fonctionnelle était assuré par un aminothiol, qui joue le rôle d’espaceur.
L’acide folique a plusieurs fonctions, dont la reconnaissance des cellules malignes.
Des études ont récemment montré que les cellules cancéreuses avaient en général la particularité de sur-exprimer un récepteur appelé “récepteur folate”. Les cellules cancéreuses développent sur leur surface un très grand nombre de sites de reconnaissance à l’acide folique qui permettront de créer des liaisons covalentes avec les cellules malignes.
Après que la molécule ait pénétré la cellule, on peut provoquer sa destruction de différentes façons.

Les nanobilles, la résonance plasmonique
En 1998, deux chercheuses de Rice University à Houston, Jennifer West et Naomi Halas, avaient remarqué que sous l'effet d'un laser, des nanobilles (nanoshells), billes de silice enrobées d'or, pas plus grosses que quelques dizaines de millionièmes de millimètre, émettent un rayonnement, d'une longueur d'onde différente, qui dépend du rapport entre la taille du noyau de silice et l'épaisseur de la couche d'or.
Ce phénomène physique était connu depuis les années 1950 sous le nom de résonance plasmonique, mais n’avait jamais été observé sur de tels objets hybrides.
De plus, aux fréquences lumineuses proches de l'infrarouge (autour de 800 nanomètres), le rayonnement peut traverser les tissus biologiques qui sont transparents à ces fréquences.
La photothermie ou hyperthermie
Jennifer West va immédiatement entrevoir l'utilité de cette propriété : si ces particules parviennent au contact de cellules tumorales et qu'elles augmentent leur température normale (37°C) d'une dizaine de degrés seulement, elles pourraient détruire les tumeurs.
Il s'agissait de petites particules de silice de 110 nm de diamètre, recouvertes d'une couche d'or de 10 nm d’épaisseur qui s’échauffe quand une lumière se situant dans l'infrarouge proche est envoyée. En fixant des anticorps spécifiques des antigènes de la tumeur cancéreuse, on fabrique un système de nanobilles capable de cibler exclusivement les cellules cancéreuses.
Le groupe du Pr West a par exemple pu, avec son système de nanoparticules en or, détruire des types de cancers inopérables.
La technique a été expérimentée dès 2004 sur des patients souffrant de graves cancers du poumons.
L’équipe de Mostafa El-Sayed (Georgia Institute of Technology) a obtenu des résultats similaires en utilisant des nanoaiguilles d’or au lieu d’une structure core/shell silice/or.
L'énergie de résonance, qui est spécifique de la nanoparticule, est fournie par un laser. A la résonance, la vibration provoque une élévation locale de température qui peut léser la tumeur de trois façons :
- par mort cellulaire en perçant des trous dans la membrane cytoplasmique des cellules cancéreuses, ce qui provoque un déséquilibre des fluides intra et extracellulaires et l'explosion de la cellule.
- Par dénaturation de l'ADN indispensable aux mitoses des cellules cancéreuses, ce qui empêche la réplication des cellules et donc la croissance de la tumeur.
- En bloquant la formation de nouveaux vaisseaux ; en effet, la dangerosité des tumeurs provient de leur capacité à construire leurs propres vaisseaux (angiogénèse), augmentant ainsi leur irrigation sanguine et donc leur apport de nutriments. En dénaturant l'ADN des cellules, leur différenciation en vaisseaux sanguins est impossible. La cellule cancéreuse, privée de ces apports, sera plus vulnérable et mourra.

Activation magnétique des cellules tumorales
Il faut noter que plusieurs types de nanoparticules peuvent également être activés à distance, par un champ magnétique par
exemple. En Allemagne, l’équipe berlinoise du Pr Maier-Hauff a ainsi soigné un glioblastome (une tumeur cérébrale) ainsi qu’une tumeur cancéreuse sous-claviculaire, après avoir injecté localement des
nanoparticules magnétiques à base de fer.
Ces nanoparticules, absorbées plus rapidement dans les cellules tumorales que dans les cellules saines, ont été chauffées grâce à un champ magnétique extérieur. Les cellules tumorales soumises à un tel traitement (qui porte la température à 45°) pendant deux ou trois heures ont bien été détruites.
Exemple de nanovecteurs de 3ème génération (figure ci-dessous)
Les nanocapsules de troisième génération, c'est à dire des nanocapsules sur lesquelles on a fixé des polymères hydrophiles comme par exemple du polyéthylène glycol (PEG.), puis que l’on a ensuite ornées d’acide folique, sont injectées au patient par voie intraveineuse.
On les appelle des nanovecteurs furtifs car l’organisme ne les reconnaît pas comme étant des corps étrangers.
En arrivant à proximité d’une tumeur, les nanovecteurs se fixent sélectivement sur les cellules cibles malades, porteuses du récepteur à l’acide folique. Ils sont ensuite transportés à l’intérieur de la cellule par endocytose. Le principe actif est alors délivré dans la cellule cancéreuse.
Les laboratoires de poche, labopuces/ Lab on Chip

Les labopuces (Lab on Chip)
Les biopuces sont des systèmes miniaturisés dédiés à l'étude d'échantillons biologiques. Elles mettent en œuvre un élément de transduction du signal, couplé à un motif de reconnaissance (ADN, anticorps, polymère...) dont la liaison avec la molécule cible qui lui est spécifique génère un signal
Le labopuce est un dispositif portable qui permet, en quelques dizaines de minutes et à partir de quelques gouttes de sang, de salive ou d’urine, de réaliser sur une surface de quelques centimètres carrés, une véritable analyse biologique.
Une étude récente, publiée en août 2011 dans la revue Nature Medicine, décrit l'utilisation de prototypes d’une biopuce (mChip), de la taille d'une carte bancaire, testée sur des centaines d'analyses au Rwanda.
mChip est capable de dépister différentes protéines, révélatrices des maladies qui
leurs sont liées, dans un seul échantillon de sang. Pour lire le résultat, il suffit d'un détecteur coûtant une centaine de dollars
seulement.
Ces chercheurs seraient parvenus à un taux de détection dont la précision approche les 100%. Le dispositif utilise des nanoparticules d'or et d'argent couplées à une puce électronique, le tout enfermé dans un boîtier plastique.
Le coût de production estimé de ce laboratoire d'analyse de sang miniaturisé, ne dépasserait pas un dollar
pièce, une solution idéale pour les patients des régions les plus pauvres du monde.
Le concepteur de cette biopuce, Samuel Sia, enseignant à l'Université américaine de Columbia écrit :
"L'idée est de produire un grand éventail de tests accessible à n'importe quel type de patients dans le monde, plutôt que de
les contraindre à se rendre dans une clinique pour un prélèvement de sang et à attendre les résultats des jours et des jours (concepteur de cette biopuce).
L’intérêt de ce dispositif réside aussi dans le fait qu’une dizaine de pathologies différentes peuvent être dépistées
simultanément, l'appareil détectant de manière distincte les "marqueurs" biologiques de ces maladies.
NB : ICI un labpuce récent destiné à tester des produits alimentaires.
A LIRE :
- GdR Or-nano, ressources documentaires,
- World Gold Council, Technology,
- Les nanoparticules d'or, un remède contre le cancer



