- AVANT-PROPOS
- A la UNE
- PRESENTATION
- ACTUALITE SCIENTIFIQUE et TECHNOLOGIQUE
- ACTUALITE ARTISTIQUE
- BLOG
- CONSCIENCE
- PLANETE VIVANTE
- SCIENCES
- Sciences et histoire
- Science et politique
- Science/conscience
- Médecine de demain
- Le COVID-19
- COVID-19 - Journal d'une pandémie - 1 -
- COVID-19 - Journal d'une pandémie - 2 -
- COVID-19 - Journal d'une pandémie - 3 -
- COVID-19 - Journal d'une pandémie - 4 -
- COVID-19 - Journal d'une pandémie - 5 -
- COVID-19 - Journal d'une pandémie -6 -
- COVID-19 - Journal d'une pandémie - 7
- COVID-19 - Journal d'une pandémie - 8
- COVID -19 - Journal d'une pandémie - 9
- COVID-19 - Journal d'une pandémie - 10
- COVID-19 - Journal d'une pandemie - 11
- Arts et sciences
- L'homme debout
- Les débuts de la sagesse
- L'épopée scientifique
- Chimie, vivant... une si longue histoire !
- Introduction : 52 choses que je sais d'elle
- Sommaire
- 1 - Premiers pas
- I - A l'origine
- II - De la tetrasomia et l'alchimie à la chimie moderne
- III - al-kimiya
- IV - Alchimie : de l'aube à la fin de la Renaissance
- V - De l'(al)chimie à la chimie : une question de méthode ?
- VI - L'alchimie selon Newton, première partie
- VII - L'alchimie selon Newton, deuxième partie
- 2 - La chimie des Lumières
- XI - Chimie au siècle des Lumières - Introduction
- XII - Chimie au siècle des Lumières- Les affinités électives
- XIII - Diderot et la chimie
- XIV - Diderot - La chimie, pourquoi ?
- XV- Diderot chimiste
- XVI- La chimie et le Rêve de D'Alembert
- 3 - La chimie du vivant
- X - Chimie et Vivant - Introduction
- XIX - La génération spontanée
- XX - Fermentation : duel à 3 !
- XXI - Stéréochimie : clé du Vivant
- XXII - Homochiralité et origine de la vie
- XXIIc - Origine de la vie : état des lieux... provisoire
- XXIIb - Des biopolymères aux premiers organismes vivants
- XXIII- Stéréochimie et activité biologique
- XXIV - Chimie du cerveau - 1- Un cerveau, trois cerveaux, des cerveaux...
- XXV - Chimie du cerveau - 2 - Les neurotransmetteurs, messagers chimiques
- XXVI- Chimie du cerveau -3- Rôle des différents neurotransmetteurs
- XXXIV - Odorat, Odeurs et parfums
- XXXV- Bonnes et mauvaises odeurs
- XXXVI - Chimie et parfums
- XLIII - Chimie et couleur -1- De colore
- XLIV - Chimie et couleur -2- Couleurs végétales
- XLV - Chimie et couleur -3- : chimiothérapie et colorants
- XL- a - ADN, ARN, protéines
- XL- b - Chimie supramoléculaire
- XXXIX- Chimie et Synthetic Biology
- XLVI - Du génome au protéome
- 4 - Chimie et médecine
- VIII - Chimie et médecine : d'Hippocrate à Néron
- IX - Chimie et opium : voyages, voyages !
- XVII- Médecine et Chimie à Montpellier avant la Révolution
- XVIII - Le vitalisme de l'Ecole de Montpellier
- XXIX - Le médicament aujourd'hui
- XXVII - Autour de la sérotonine
- XXVIII - L'ocytocine
- XXX - Chimie, médecine, nanotechnologies
- L - Chimie et dopage -1- La chimie au service du dopage
- LI - Chimie et dopage - 2 - Les outils du chimiste contre le dopage
- XLIX - Image magnétique - 3 - de l'IRM au patient numérique
- 5 - La chimie moderne et ses hommes
- XXXI - Mendeleïev : un tableau de maître !
- XXXII - Mendeleïev : -2- Un chimiste russe au XIXème siècle
- XXXIII - Mendeleïev -3- Le fin mot de l'histoire
- XLI - Paul Sabatier, chimiste languedocien, prix Nobel 1912
- XLII - Victor Grignard, prix Nobel 1912
- XLVII - Image magnétique - 1 - Une histoire de spin
- XLVIII - Image magnétique - 2 - Mais que vient faire le chimiste dans cette galère ?
- 6 - Chimie : bonnes et mauvaises pratiques
- XXXVII- Du mauvais usage de la chimie
- XXXVIII- La chimie passe au vert
- Pour conclure
- Postface - Nylon by DuPont de Nemours
- Nylon... - Part A
- Nylon... - Part B
- Nylon... - Part C
- Nylon... - Part D
- La beauté des mathématiques
- Les sciences vers La Science
- La révolution numérique
- CRISPR-Cas9 : l'édition de gènes
- L'ombre de Frankenstein
- VOIR
- RECHERCHE, CONTACT
L'Imagerie par résonance magnétique (IRM)

A partir du moment où la RMN 2D a commencé à fournir une véritable cartographie de molécules complexes avec la mise en oeuvre des différentes séquences décrites précédemment, il était évident que les spécialistes de l'imagerie médicale allaient entrer en piste.
En effet de quoi sont principalement constitués nos tissus ?
D'eau !
L'eau c'est deux atomes d'hydrogène liés à un atome d'oxygène (H2O). Pourquoi donc ne pas tenter de faire de la RMN du proton sur un corps humain, essayer ensuite de différencier les signaux obtenus pour les transformer en image par les moyens informatiques de traitement de données.
La RMN devient alors IRM, sigle qui a l'avantage d'escamoter le N de nucléaire qui pourrait faire peur aux patients... alors que nous l'avons vu, l'énergie mise en jeu dans une expérience de RMN est dérisoire, surtout si on la compare à un cliché de RX.
Peter Mansfield et Paul Lauterbur ( prix Nobel de physiologie ou médecine en 2003) ont été les premiers à produire des images à partir de la RMN.
MAIS COMMENT FABRIQUER UNE IMAGE ?

La réalisation d'une IRM c'est en gros une expérience de RMN telle que je l'ai décrite précédemment.
L'échantillon (un corps humain) est introduit dans un tube de 60 cm de diamètre environ, siège d'un puissant champ magnétique constant produit par un aimant supraconducteur pouvant atteindre 10 Teslas (bientôt plus).
Tous les spins se mettent alors à tourner comme des toupies !
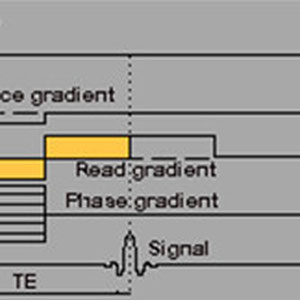
Un champ oscillant est créé pendant un temps très bref par des bobines de gradient de champ (réparties autour du tube) dans les trois directions de l'espace pour provoquer l'excitation des noyaux.
Après l'arrêt de cette impulsion, les noyaux reviennent à leur position initiale, c'est ce que l'on appelle la relaxation. L'expérience est répétée, une antenne réceptrice enregistre les signaux de précession des atomes qui résonnent dans la zone explorée.
Un puissant ordinateur va traiter les signaux obtenus (c'est à dire une très grande quantité de données !) et reconstituer une image en trois dimensions.
En résumant d'une façon grossière, on peut dire qu'au cours d'une IRM, on mesure l'aimantation résultante en chaque point des tissus analysés. Comme cette aimantation est proportionnelle à la quantité de noyaux d'hydrogène présents, et que les tissus se distinguent par leur contenu en eau, la carte des aimantations résultantes reproduit l'anatomie de ces tissus.
L'obtention d'une image nécessite donc 5 étapes :
1) Exciter la matière (les protons)
2) Encoder la position avec un gradient de champ
3) Recueillir un signal d’écho avec une antenne
4) Décoder la position avec la transformée de Fourier
5) Dessiner la zone correspondant à cette position avec une teinte ± claire selon la quantité de signal

Joseph Fourier est le grand magicien de la RMN et de l'IRM !
Ce génial mathématicien français a démontré que toute fonction peut-être décomposée en une suite de fonctions cycliques et explicité les formules qui permettent d'en retrouver les fréquences.
Ce qu’on appelle l’analyse de Fourier d’un signal, ou d’une image, ou de toute autre variable, consiste donc à calculer les fréquences qui composent ce signal (ou cette image), ainsi que les amplitudes associées qui ne sont en fait que leurs facteurs de pondération.
En IRM, la fonction représente l'état du champ électromagnétique (le signal) et sa transformée de Fourier est son image.
Lorsque le système récupère le signal il remplit donc un espace mathématique qui est appelé espace de Fourrier ou espace des K.
Cet espace K va contenir toutes les informations nécessaires à la formation de l'image.
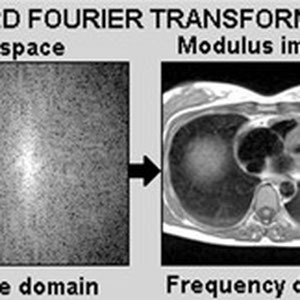
On passe ensuite de l'espace K à l'image par transformée de Fourier
C'est ce que résument les 3 diapos ci-dessous (image cardiaque) :
L'IRM fait des petits !
L’imagerie par résonance magnétique est donc capable d’étudier des tissus dits mous, tels que le cerveau, la moelle épinière, les muscles... et de donner une imagerie morphologique avec un grand contraste tissulaire.
Elle donne une structure anatomique (IRM anatomique, IRMa), mais permet aussi de suivre une fonction (IRMf) ou d'étudier le métabolisme (spectroscopie IRM, SRM).
L’IRMa , la plus utilisée, offre la possibilité de visualiser l’anatomie d’organes profonds et opaques. Elle permet en particulier de visualiser le cerveau en coupes montrant les détails des structures cérébrales (matière grise, matière blanche) avec une précision millimétrique.
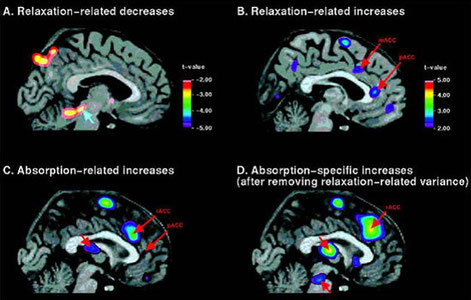
L’IRMf dite fonctionnelle est plus récente. Grâce à la vitesse d’acquisition et de traitement de données on peut révéler l’activité des différentes structures qui composent le cerveau.
L'IRM fonctionnelle ne détecte pas l'activation absolue des régions du cerveau. Elle met en évidence des différences d'activations selon différentes conditions opératoires.
Pendant l'acquisition des images, le patient est stimulé, on lui demande d'accomplir des tâches, on suscite des émotions... on alterne périodes de stimulation et période de repos.
La combinaison des ces différentes conditions est appelée un paradigme d'IRM fonctionnelle. Les stimuli sont en général présentés grâce à un système audio-visuel, mais peuvent utiliser des systèmes plus complexes (odorat, goût,etc.).
La détection des aires cérébrales sollicitées durant l'expérience est basée sur l'effet BOLD (Blood Oxygenation Level Dependent).
Dans les zones activées, une petite augmentation de la consommation d'oxygène est sur-compensée par une large augmentation de flux sanguin. Il en résulte une diminution du rapport déoxy-/oxy-hémoglobine. La déoxyhémoglobine est paramagnétique, quand sa concentration diminue le signal augmente sur l'image IRMf. Le signal dans les zones activées varie en fonction du paradigme.
En résumé, lors de l'IRMf on enregistre le « signal BOLD » en temps réel sur un patient et l'on suit en direct l’oxygénation du cerveau lors d’exercices cognitifs, qui mettent ainsi en évidence les zones qui sont actives.
Cette technique a permis de très grandes avancés pour la recherche en psychologie cognitive et comportementale, ainsi qu’en psychiatrie, dans les dix dernières années.
L’IRMf a détrôné la TEP (Tomographie par Emission de Positrons) jusqu’alors utilisée, technique invasive, générant des radiations, et dont la résolution est moindre.
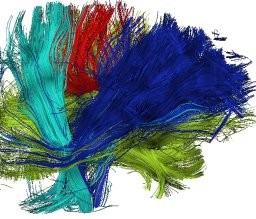
L’IRMd de diffusion (IRMd). C’est un outil puissant pour mesurer les micro-mouvements des molécules d’eau et établir ainsi l’architecture fine du tissu neuronal et ses variations. Elle donne une mesure plus directe et bien plus fine que les méthodes d’imagerie classiquement utilisées. Elle permet d’observer la connectivité cérébrale in vivo de manière non invasive.
La tractographie est sa dernière évolution, elle offre la possibilité d’étudier in vivo la substance blanche du cerveau.
Enfin, la spectroscopie par résonance magnétique nucléaire (SRM) complète cette palette de technologies, en fournissant une méthode non invasive d’étude de la biochimie et du métabolisme du système nerveux central. Elle permet la quantification précise de plusieurs dizaines de molécules.
La mesure de ces flux métaboliques cérébraux par spectroscopie par SRM, connait un développement considérable. Par exemple, la SRM du phosphore 31 permet la mesure directe du flux cérébral de synthèse d'ATP.
Le rêve et son interprétation : de Freud à l'IRM fonctionnelle
" Je rêvais que j’étais un papillon volant dans les airs et ne sachant rien de Chuang Tzu "

Je n'ai pas les compétences pour discuter du travail de Freud -contesté par certains aujourd'hui.
On pourra aller ICI, sur un lien qui traite du sujet à un niveau scolaire, que je n'ai pas dépassé !
Sa lecture est en tout cas fort utile.
Ce qui n'est pas discutable par contre, c'est ce que commence à montrer l'imagerie cérébrale (dont je parle beaucoup sur ce site) à propos de l'empreinte des rêves sur notre cerveau.
Depuis quelques années, de nombreuses études étonnantes sont publiées dans les grandes revues scientifiques.
Les chercheurs japonais sont en pointe dans ce domaine.
Une équipe de l'ATR Computational Neuroscience Laboratories à Kyoto a décrit pour la première fois en 2013, des rêves, sur la base d'images cérébrales réalisées par IRMf, en tandem avec l'électroencéphalographie (EEG).
Dans ces conditions, ils ont été en mesure de décrire ce que les cobayes avaient rêvé avec 60% de précision, un taux beaucoup plus élevé que ce qui peut être attribué au hasard. Bluffant !
L'imagerie computationnelle : c'est déjà demain !
Bénie soit l'informatique... et les informaticiens !

Nous venons de voir que l'informatique occupe le point central de la RMN et de l'IRM. Les progrès prodigieux de l'imagerie médicale sont directement liés aux capacités de traitement de quantités faramineuses de données.
La plupart des images médicales sont très volumineuses. L’image anatomique d’un organe, voire du corps entier peut contenir entre quelques millions et plusieurs centaines de millions de voxels (extension volumique du pixel).
La quantité d’information augmente rapidement lorsque plusieurs images sont acquises sur un même patient pour exploiter la complémentarité des différentes modalités, ou pour suivre une évolution temporelle ; il s’agit alors d’images 4-D avec trois dimensions spatiales et une dimension temporelle.
La question qui est posée au clinicien, au chirurgien, à la médecine en général, est de comment exploiter au mieux toute la masse des informations recueillies.
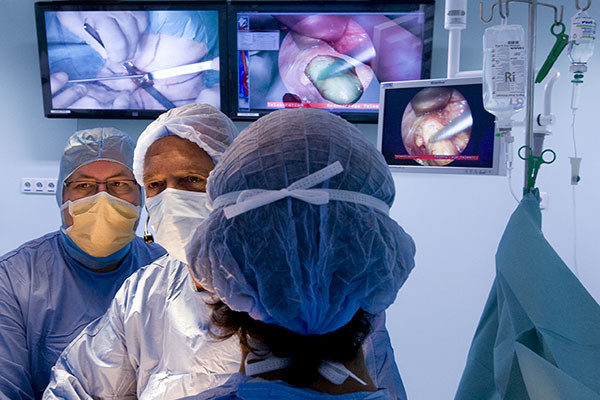
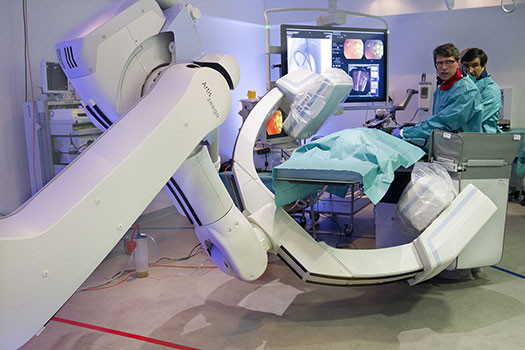
Une nouvelle discipline est donc en train d'émerger : l'imagerie computationnelle, dont Nicholas Ayache, directeur de recherche à l'Inria (Institut national de recherche en informatique et automatique) à Sophia Antipolis, mais aussi directeur scientifique de l'Institut hospitalo-universitaire (IHU) de Strasbourg, depuis sa création en janvier 2012, est le plus éminent représentant.
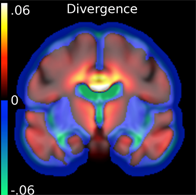
L’informatique et les sciences numériques vont en effet jouer un rôle crucial pour exploiter de façon rigoureuse et optimale cette surabondance d’information.
Elles sont essentielles pour l’analyse des images reconstruites dont le but est d’extraire de façon objective toute l’information cliniquement pertinente au médecin.
Elles vont permettre de construire un modèle numérique du patient pour la simulation : simulation
de l’évolution d’une pathologie ou de l’effet d’une thérapie par exemple, ou simulation de gestes médicaux ou chirurgicaux pour l’entraînement du praticien.
En souvenir du Docteur Robert Ollé
2016, U.K. : lancement de la plus vaste étude en imagerie biomédicale
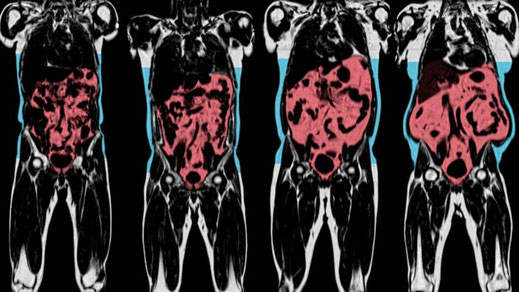
La société à but non lucratif Biobank (UK) va lancer la plus vaste étude d'analyse en imagerie médicale jamais entreprise.
Un référentiel de données biologiques concernant les organes de 100 000 personnes suivies par imagerie de résonance magnétique (et autres techniques standard), pendant les 6 à 8 prochaines années, va être établi.
Il sera corrélé avec d'autres paramètres comme la santé et le style de vie.
Cela devrait permettre aux chercheurs d'améliorer la compréhension, le diagnostic et le pronostic de maladies comme le cancer, la démence, l'arthrite...