- AVANT-PROPOS
- A la UNE
- PRESENTATION
- ACTUALITE SCIENTIFIQUE et TECHNOLOGIQUE
- ACTUALITE ARTISTIQUE
- BLOG
- CONSCIENCE
- PLANETE VIVANTE
- SCIENCES
- Sciences et histoire
- Science et politique
- Science/conscience
- Médecine de demain
- Le COVID-19
- COVID-19 - Journal d'une pandémie - 1 -
- COVID-19 - Journal d'une pandémie - 2 -
- COVID-19 - Journal d'une pandémie - 3 -
- COVID-19 - Journal d'une pandémie - 4 -
- COVID-19 - Journal d'une pandémie - 5 -
- COVID-19 - Journal d'une pandémie -6 -
- COVID-19 - Journal d'une pandémie - 7
- COVID-19 - Journal d'une pandémie - 8
- COVID -19 - Journal d'une pandémie - 9
- COVID-19 - Journal d'une pandémie - 10
- COVID-19 - Journal d'une pandemie - 11
- Arts et sciences
- L'homme debout
- Les débuts de la sagesse
- L'épopée scientifique
- Chimie, vivant... une si longue histoire !
- Introduction : 52 choses que je sais d'elle
- Sommaire
- 1 - Premiers pas
- I - A l'origine
- II - De la tetrasomia et l'alchimie à la chimie moderne
- III - al-kimiya
- IV - Alchimie : de l'aube à la fin de la Renaissance
- V - De l'(al)chimie à la chimie : une question de méthode ?
- VI - L'alchimie selon Newton, première partie
- VII - L'alchimie selon Newton, deuxième partie
- 2 - La chimie des Lumières
- XI - Chimie au siècle des Lumières - Introduction
- XII - Chimie au siècle des Lumières- Les affinités électives
- XIII - Diderot et la chimie
- XIV - Diderot - La chimie, pourquoi ?
- XV- Diderot chimiste
- XVI- La chimie et le Rêve de D'Alembert
- 3 - La chimie du vivant
- X - Chimie et Vivant - Introduction
- XIX - La génération spontanée
- XX - Fermentation : duel à 3 !
- XXI - Stéréochimie : clé du Vivant
- XXII - Homochiralité et origine de la vie
- XXIIc - Origine de la vie : état des lieux... provisoire
- XXIIb - Des biopolymères aux premiers organismes vivants
- XXIII- Stéréochimie et activité biologique
- XXIV - Chimie du cerveau - 1- Un cerveau, trois cerveaux, des cerveaux...
- XXV - Chimie du cerveau - 2 - Les neurotransmetteurs, messagers chimiques
- XXVI- Chimie du cerveau -3- Rôle des différents neurotransmetteurs
- XXXIV - Odorat, Odeurs et parfums
- XXXV- Bonnes et mauvaises odeurs
- XXXVI - Chimie et parfums
- XLIII - Chimie et couleur -1- De colore
- XLIV - Chimie et couleur -2- Couleurs végétales
- XLV - Chimie et couleur -3- : chimiothérapie et colorants
- XL- a - ADN, ARN, protéines
- XL- b - Chimie supramoléculaire
- XXXIX- Chimie et Synthetic Biology
- XLVI - Du génome au protéome
- 4 - Chimie et médecine
- VIII - Chimie et médecine : d'Hippocrate à Néron
- IX - Chimie et opium : voyages, voyages !
- XVII- Médecine et Chimie à Montpellier avant la Révolution
- XVIII - Le vitalisme de l'Ecole de Montpellier
- XXIX - Le médicament aujourd'hui
- XXVII - Autour de la sérotonine
- XXVIII - L'ocytocine
- XXX - Chimie, médecine, nanotechnologies
- L - Chimie et dopage -1- La chimie au service du dopage
- LI - Chimie et dopage - 2 - Les outils du chimiste contre le dopage
- XLIX - Image magnétique - 3 - de l'IRM au patient numérique
- 5 - La chimie moderne et ses hommes
- XXXI - Mendeleïev : un tableau de maître !
- XXXII - Mendeleïev : -2- Un chimiste russe au XIXème siècle
- XXXIII - Mendeleïev -3- Le fin mot de l'histoire
- XLI - Paul Sabatier, chimiste languedocien, prix Nobel 1912
- XLII - Victor Grignard, prix Nobel 1912
- XLVII - Image magnétique - 1 - Une histoire de spin
- XLVIII - Image magnétique - 2 - Mais que vient faire le chimiste dans cette galère ?
- 6 - Chimie : bonnes et mauvaises pratiques
- XXXVII- Du mauvais usage de la chimie
- XXXVIII- La chimie passe au vert
- Pour conclure
- Postface - Nylon by DuPont de Nemours
- Nylon... - Part A
- Nylon... - Part B
- Nylon... - Part C
- Nylon... - Part D
- La beauté des mathématiques
- Les sciences vers La Science
- La révolution numérique
- CRISPR-Cas9 : l'édition de gènes
- L'ombre de Frankenstein
- VOIR
- RECHERCHE, CONTACT
Le prix Nobel de physiologie ou médecine 2024 : encore l'ARN...
... mais les microARN


Les ARN les plus étudiés étaient essentiellement :
- les ARN messagers (ARNm), qui portent l'information nécessaire à la synthèse des protéines, ainsi que - les ARN ribosomiques (ARNr)
- et les ARN de transfert (ARNt), qui fabriquent les protéines à partir de l'information des ARNm.
Depuis 20 ans, les biologistes ont découvert trois nouvelles classes d'ARN : les microARN, les siARN et les piARN. À l'inverse des ARNm, ces nouveaux ARN ne codent pas de protéines, ils jouent un rôle en contrôlant l'expression d'autres gènes.
Victor Ambros et Gary Ruvkun ont travaillé sur l’organisme modèle Caenorhabditis elegans. Ce ver rond d’environ 1 millimètre de long possède différents types cellulaires: pour les muscles, pour le système nerveux et pour le système digestif. Cette organisation simplifiée en fait un organisme modèle pour l’étude du développement des pluricellulaires.
Dans les années 1980 et 1990, les deux biologistes cherchent à comprendre les processus qui régissent la croissance de ce petit nématode transparent. Ils découvrent alors un nouveau mécanisme de régulation des gènes. En 1993, ils publient dans la prestigieuse revue Cell leurs premiers résultats sur les micro-ARNs.
Cela justifie le prix Nobel qui leur a été décerné hier.
Il s'agit encore une fois d'un travail de recherche fondamentale qui débouche sur des applications très importantes pour la santé humaine.
Les études fonctionnelles réalisées sur les micro-ARN indiquent en effet que ces petits ARN (pas plus de 25 nucléotides, c'est à dire pas plus de 25 bases nucléiques) participent à la régulation de quasiment tous les processus cellulaires.
Ainsi, les micro-ARN inhibent l’expression de gènes en provoquant la dégradation de leur ARN messager. Un seul micro-ARN peut réguler l’expression de nombreux gènes différents. Et, inversement, un seul gène peut être régulé par plusieurs microARN.
Ils jouent un rôle majeur dans les processus de développement et de maintien de la différentiation. De plus, des altérations dans leur niveau d’expression ont été associées à bon nombre de pathologies (cancers, maladies cardiovasculaires, inflammatoires…).
Les études fonctionnelles de certains miARN impliqués dans la carcinogenèse ont permis d’identifier certains d’entre eux comme d’authentiques oncogènes ou gènes suppresseurs de tumeurs.
Des traitements basés sur le microARN sont en cours d’essais cliniques pour les maladies cardiaques, le cancer et les maladies neurodégénératives.
Outre leur rôle dans la cancérogenèse, les micro-ARN constituent des biomarqueurs pronostiques et diagnostiques prometteurs dans les cancers.
"Certes, c’est toujours un accomplissement pour un chercheurs lorsque sa recherche a des applications. Mais il ne faut pas négliger l’importance de la recherche fondamentale. D’ailleurs, un chercheur ne perd jamais de vue l’appliqué. Il est nécessaire de continuer à explorer notre curiosité initiale sans se limiter aux applications"
Anne Houdusse-Juille, directrice de recherche CNRS à l’Institut Curie et membre de l’Académie des sciences
MARS 2023
Il y a 70 ans, découverte de la structure de l'ADN
Le 25 avril 1953, un article de James Watson et Francis Crick, publié dans la revue Nature, révolutionne la biologie et la médecine.

RAPPEL
L'ADN est composé de séquences de nucléotides. Chaque nucléotide est un assemblage de trois éléments :
- un groupe phosphate lié à un sucre, le désoxyribose, lui-même lié à une base azotée.
Quatre bases azotées sont concernées : l'adénine (A), la thymine (T), la cytosine (C) et la guanine (G).
Dans l'ADN, les nucléotides sont reliés entre eux selon une certaine séquence grâce à des liaisons impliquant un groupe phosphate. Un brin d'ADN est obtenu par l'enchaînement des nucléotides via des liaisons fortes.
L'ADN est composé en fait de deux brins se faisant face, et formant une double hélice. Cette structure supramoléculaire est obtenue grâce à des liaisons faibles : les liaisons "hydrogène".
Il y a deux liaisons hydrogènes entre A et T et trois entre C et G. En face d'une adénine, il y a toujours une thymine; en face d'une cytosine, il y a toujours une guanine.
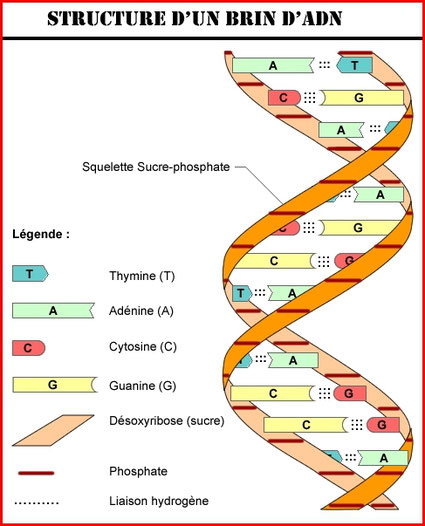
Les auteurs établissent dans cet article la structure à double hélice de l’acide désoxyribonucléique (ADN), permettant de comprendre l’ensemble du fonctionnement génétique d’êtres vivants.
De cette découverte en découleront d’autres qui deviendront indispensables.
En 1944, Oswald Avery identifie la substance qui compose les chromosomes : l’acide désoxyribonucléique (ADN).
En 1950, Edwin Chargaff découvre que l’ADN, est composé de quatre types de molécules nommés nucléotides : l’adénine (A), la thymine (T), la cytosine (C) et la guanine (G).
Malgré ces connaissances fondamentales, les scientifiques ignorent toujours ce qui relie et assemble les molécules.
Au cours des années 1950, plusieurs équipes de recherche tentent donc de comprendre l’ADN.
L’une d’elles, formée du biologiste américain James Watson et du physicien britannique Francis Crick, publie un article dans la revue Nature le 25 avril 1953. Il démontre que la structure de l’ADN est à double hélice.
Cette découverte est fondée sur une synthèse des différentes connaissances, notamment des travaux d’observation de diffraction des rayons X de Maurice Wilkins et de Rosalind Franklin, ainsi que l’idée d’association de bases azotées. Elle bouleversera l’histoire de la biologie, plus précisément de la génétique.
Les résultats signifient qu’il est désormais possible pour les scientifiques d’expliquer comment se fait la transmission de l’information génétique pour la matière vivante. Cette découverte vaut à Crick, Watson et Wilkins le prix Nobel de la physiologie et de la médecine en 1962.
Elle permettra de comprendre l’ensemble des mécanismes moléculaires génétiques (réplication, transcriptions, etc.). Elle rend également possible le décodage du code génétique, c’est-à-dire la possibilité d’isoler des gènes ou d’introduire des structures dans l’ADN à des fins médicales.
C’est grâce au travail de ces chercheurs qu’il a été possible de séquencer le génome humain.
SUR CE SITE :
- des biopolymères aux premiers organismes vivants,
- CRISPR-CAS9, l'édition des gènes,
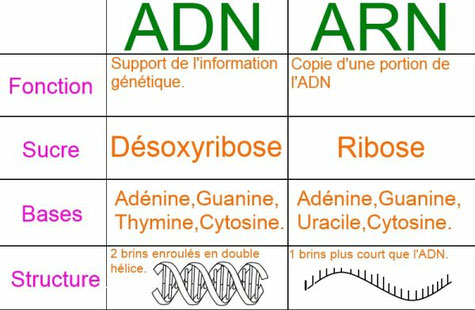
Si l’ADN est le support de l’hérédité, c’est l’ARN, l’acide ribonucléique, qui est généralement utilisé dans les cellules comme intermédiaire des gènes pour fabriquer les protéines dont elles ont besoin. L’ARN intervient aussi dans nombre de réactions chimiques de la cellule.
D’un point de vue évolutif, on pense que l’ARN serait antérieur à l’ADN comme support de l’information génétique, ce qui expliquerait ses fonctions plus étendues et sa généralisation. L’ADN serait apparu plus tard en raison de sa plus grande stabilité.
Les associations moléculaires derrière la forme

Les chercheurs utilisent les nouvelles technologies pour percer les détails de cette extraordinaire construction.
On sait que les associations moléculaires sont essentielles, Qu'il s'agisse de modifications de la disposition topologique des régions chromosomiques qui rapprochent une partie du génome d'une autre, ou d'une modification chimique de nucléotides, ou de protéines, qui modulent la distance de la liaison aux protéines, influençant ainsi l'état de la chromatine.
Les chaperons d'histones et les remodeleurs contribuent également à la polyvalence du paysage génétique et épigénétique en choisissant un destin cellulaire spécifique lorsque les cellules sont soumises à des conditions environnementales variées, à des changements métaboliques ou même à des maladies.
Régulation des gènes et développement
Shaping the body - Façonner l'organisme


Dans l'art des "ballons", le sculpteur exerce des forces précises sur des sites spécifiques pour fabriquer des éléments corporels. De même, les mécanismes moléculaires, bien que de niveau complexe et étroitement contrôlés, permettent à quelques cellules de départ, apparemment identiques, de se transformer en un animal entier. Un numéro spécial de la revue Science, met en évidence les mécanismes de régulation contrôlant l'expression des gènes (décrits ci-dessus en arrière-plan, sous la forme d'une carte thermique).
Quelles sont donc les forces qui sont à l'oeuvre derrière la forme ?
Ce sont des programmes génétiques précis et très sophistiqués qui guident les forces qui permettent à des cellules initiales de se développer en entités hautement spécialisées, comme par exemple, un cardiomyocyte contractile, une cellule bêta pancréatique sécrétant l'insuline, une rétine sensible à la lumière ou un os...
Mais quels sont donc les facteurs et les mécanismes qui sont en jeu ? C'est une question qui anime les travaux de nombreuses équipes de recherche, comme celle de Geneviève Almouzni à l'Institut Curie (Paris).
ADN, chimie, vivant ; après le Nobel de chimie 2015
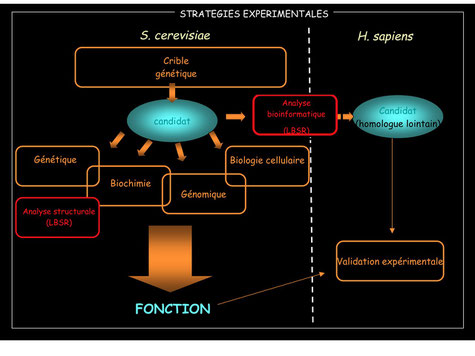
Le prix Nobel de chimie 2015 met en lumière, si besoin était, le travail fondamental des chercheurs autour de ce qui est le fondement même de la vie sur cette terre : les acides nucléiques.
Ce sont les mécanismes de réparation de l'ADN qui viennent d'être récompensés.
La chimie est au coeur de ces processus qui impliquent l'élaboration et la rupture de liaisons chimiques.
Sans la chimie, ces processus ne seraient pas possible, et la vie ne pouvaient tout simplement pas se produire.
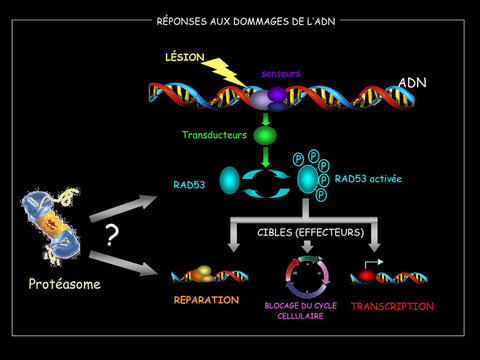
Le Prix Nobel de chimie 2015 récompense trois pionniers qui ont cartographié plusieurs de ces systèmes de réparation :
- le système de réparation par excision de base (base excision repair ou BER), découvert par Tomas Lindahl,
- le système de réparation des mésappariements (mismatch repair), identifié par Paul Modrich,
- le système de réparation par excision de nucléotides (nucleotide excision repair ou NER), cartographié par Aziz Sancar.
Ce dernier système est décrit dans le film d’animation ci-dessous, réalisé avec le soutien de l’Inserm et de l’Institut de Génétique et de Biologie Moléculaire et Cellulaire (IGBMC, Ilkirch).
On a longtemps cru que l'ADN, support de l'information génétique, était totalement inerte ; la pérennisation de la vie sur terre pendant des millions d'années semblait l'imposer.
Tomas Lindahl, l'un des trois récipiendaires de ce Nobel, après avoir mis en évidence la fragilité de l'ARN (de structure très voisine, mais possédant une fonction hydroxyle libre), fut le premier a montrer que l'ADN, soumis à de nombreux stress naturels tout au long de la vie de la cellule, peut subir des dommages.
Le métabolisme cellulaire produit notamment des espèces réactives de l’oxygène et l’environnement soumet en permanence les organismes à des agressions, comme le rayonnement ultraviolet (UV), les radiations ionisantes ou l'exposition à des agents génotoxiques (tabac par exemple).
Lindhal fut aussi pionnier dans la découverte des mécanismes de réparation dont les cellules disposent.
Lindahl. Instability and decay of the primary structure of DNA. Nature362, 709-715 (1993)
Lindahl and R.D. Wood. Quality control by DNA repair. Science 286, 1897-1905 (1999)
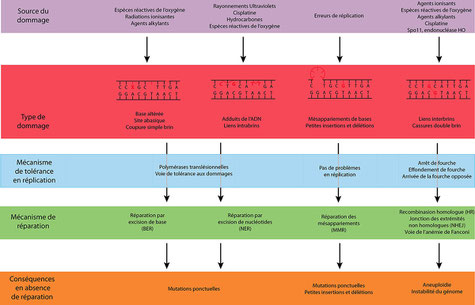
De nombreux mécanismes de réponse ont été développés par la cellule pour la prise en charge et l’élimination des différents types de lésions pouvant altérer le matériel génétique.
De plus, lorsque la lésion n’est pas réparée avant l’arrivée de la fourche de réplication, une voie de tolérance aux dommages existe afin d’empêcher un arrêt intempestif de la réplication.
La réparation de l’ADN comprend l’ensemble des voies permettant de rétablir l’intégrité de l’information génétique.
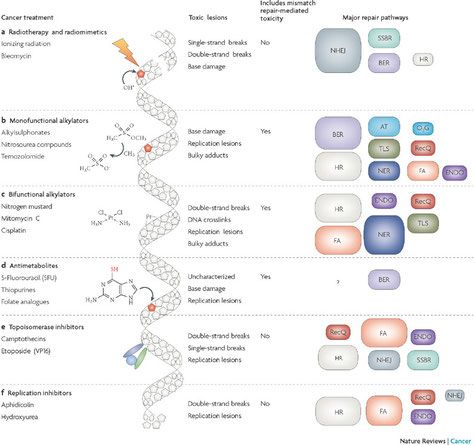
Pour conclure :
Les dommages à l’ADN font partie de la vie d’une cellule et peuvent être responsables de nombreux soucis.
Elle dispose heureusement de mécanismes de réparation complexes, spécialisés et efficaces.
Lorsque des mutations ponctuelles non réparées surviennent dans les lignées germinales, elles se transmettent et sont à l’origine de maladies génétiques, parfois redoutables.
D'autre part, la dérégulation des mécanismes de réparation et de signalisation est à l'origine de l’instabilité génétique observée dans les cancers, et participe ainsi à la carcinogénèse.
D'un autre côté, les dommages à l’ADN réparés avec des erreurs sont un moteur essentiel à l’évolution des espèces.
La recherche fondamentale sur le cancer étudie donc les processus destinés à maintenir l’intégrité du génome. Cette recherche vise à mettre en évidence, à l’échelle moléculaire, une relation entre un défaut de réparation de l’ADN et l’instabilité génétique que ce soit au niveau du nucléotide (substitution, insertion ou délétion) ou du chromosome.
L'application de cette recherche est évidente puisqu'on sait que les cellules cancéreuses utilisent des mécanismes de réparation d'ADN pour survivre. De nombreux chercheurs étudient les moyens de perturber ou de détruire les processus de réparation dans les cellules cancéreuses.
La FDA américaine et l'EMA européenne viennent ainsi d'approuver la mise sur le marché du Lynparza (poly polymérase ADP-ribose -PARP-) pour les femmes atteintes d'un cancer avancé de l'ovaire associé à des gènes BRCA défectueux.

L'horloge épigénétique/Epigenetic clock
L'âge de vos cellules/ The age of your cells
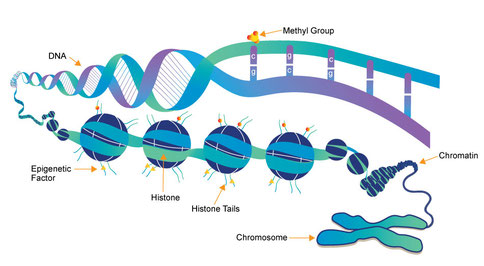
L’épigénétique correspond à l’étude des changements dans l’activité des gènes, n’impliquant pas de modification de la séquence d’ADN et pouvant être transmis lors des divisions cellulaires. Contrairement aux mutations qui affectent la séquence d’ADN, les modifications épigénétiques sont réversibles.
Un gène est un segment d’ADN qui contient l’information nécessaire à la synthèse d’une ou de plusieurs molécule(s) qui constitue(nt) l’organisme. Le gène est dit actif/allumé/exprimé lorsque cette synthèse a lieu. Sinon, il est inactif/éteint/réprimé. Mais évidemment, l’expression génétique n’est pas un processus fait de noir et blanc : il existe plein de niveau gris, avec par exemple des gènes très actifs, surexprimés (synthèse importante) ou encore partiellement réprimés (synthèse très faible)…
Les modifications épigénétiques sont induites par l’environnement au sens large : la cellule reçoit en permanence toutes sortes de signaux l’informant sur son environnement, de manière à ce qu’elle se spécialise au cours du développement, ou ajuste son activité à la situation. Ces signaux, y compris ceux liés à nos comportements (alimentation, tabagisme, stress…), peuvent conduire à des modifications dans l’expression de nos gènes, sans affecter leur séquence. Le phénomène peut être transitoire, mais il existe des modifications épigénétiques pérennes, qui persistent lorsque le signal qui les a induites disparaît.
Ces modifications sont matérialisées par des marques biochimiques, apposées par des enzymes spécialisées sur l’ADN ou sur des protéines qui le structurent, les histones.
La méthylation (fixation de groupements méthyle - CH3 = caractéristiques.un atome de carbone et trois d’hydrogène - sur l’ADN), est une de ses marques.
Les marques de méthylation localisées sur l’ADN vont le plus souvent obstruer les aires d’arrivée des complexes protéiques, conduisant ainsi à l’inactivation des gènes concernés.
Selon l'INSERM
Ci-.dessous test de traduction avec les réseaux neuronaux de DeepL, qui semblent être les plus performants.
Epigenetics refers to the study of changes in gene activity that do not involve changes in DNA sequence and can be transmitted during cell division. Unlike mutations that affect the DNA sequence, epigenetic changes are reversible.
A gene is a segment of DNA that contains the information necessary for the synthesis of one or more molecules that make up the organism. The gene is said to be active/on/expressed when this synthesis takes place. Otherwise, it is inactive/off/repressed. But obviously, gene expression is not a black and white process: there is a lot of grey level, with for example very active genes, overexpressed (important synthesis) or partially repressed (very weak synthesis)...
Epigenetic modifications are induced by the environment in the broad sense: the cell constantly receives all kinds of signals informing it about its environment, so that it specializes during development, or adjusts its activity to the situation. These signals, including those related to our behaviours (diet, smoking, stress, etc.), can lead to changes in the expression of our genes, without affecting their sequence. The phenomenon may be transient, but there are permanent epigenetic changes, which persist when the signal that induced them disappears.
These modifications are materialized by biochemical marks, affixed by specialized enzymes on DNA or on proteins that structure it, histones.
Methylation (binding of methyl groups - CH3 = characteristics.one carbon atom and three hydrogen atoms - on DNA), is one of its brands.
The methylation marks located on the DNA will most often obstruct the arrival areas of protein complexes, thus leading to the inactivation of the genes concerned.
According to INSERM
Translated with www.DeepL.com/Translator
Vieillissement et horloge épigénétique/Aging and epigenetic clock
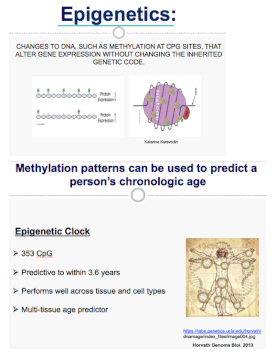
Parmi les recherches sur le vieillissement, l'épigénétique occupe une place de choix.
Les modifications chimiques apportées à l'ADN d'une personne au cours de sa vie créent ce que l'on appelle une horloge épigénétique.
Des scientifiques ont démontré que la modification dont je viens de parler - l'ajout de groupes méthyle à des séquences d'ADN spécifiques - permet de suivre l'âge biologique humain, car elle résulte de diverses pathologies, de notre environnement, de notre mode de vie et bien sûr de notre acquis génétique.
Des chercheurs ont donc établi une relation entre l'état de la méthylation de l'ADN d'une personne et son âge... et même son espérance de vie.
Par exemple, l’accélération de la méthylation de l’ADN avec l’âge est associée à la maladie d’Alzheimer à début précoce
Nous aurions de ce fait deux âges : l’âge de méthylation estimé (âge mADN) et l'âge chronologique.
Il existe aujourd’hui trois modèles d’horloges épigénétiques, à savoir les horloges de Hannum, de Weidner et de Horvath. Ces horloges diffèrent essentiellement par les sites CpG (site privilégié de méthylation) associés à l’âge, utilisés pour construire ces biomarqueurs.
Il faut savoir que ces horloges épigénétiques montrent une grande corrélation entre l’âge prédit et l’âge chronologique, avec un écart moyen de 3,6 ans pour celle d’Horvath et de 4,9 ans pour celle de Hannum.
Les horloges épigénétiques de Horvath et Hannum sont, de plus, capables de prédire la mortalité indépendamment des facteurs à risques classiques tels que l’âge, le poids, le tabagisme et l’alcoolisme, entre autres, en se basant uniquement sur les profils de méthylation des sites CpG associés à l’âge.
Enfin, l’horloge épigénétique de Horvath est aussi la seule à pouvoir s’appliquer à plusieurs tissus. En effet, elle est la première qui mesure précisément l’âge épigénétique de nos cellules, de nos tissus et/ou de nos organes, et ce de manière distincte et spécifique
Epigenetics occupies a prominent place in research on aging.
The chemical changes made to a person's DNA during their lifetime create what is called an epigenetic clock.
Scientists have demonstrated that the modification I have just mentioned - the addition of methyl groups to specific DNA sequences - makes it possible to track human biological age, because it results from various diseases, our environment, our way of life and of course our genetic heritage.
Researchers have therefore established a relationship between the state of a person's DNA methylation and their age... and even their life expectancy.
For example, the acceleration of DNA methylation with age is associated with early onset Alzheimer's disease
This would give us two ages: the estimated methylation age (mADN age) and the chronological age.
There are now three models of epigenetic clocks, namely the Hannum, Weidner and Horvath clocks. These clocks differ mainly in the CpG (privileged methylation site) sites associated with age, used to build these biomarkers.
It should be noted that these epigenetic clocks show a high correlation between predicted age and chronological age, with an average difference of 3.6 years for Horvath's and 4.9 years for Hannum's.
Horvath and Hannum epigenetic clocks are also capable of predicting mortality independently of conventional risk factors such as age, weight, smoking and alcoholism, among others, based solely on the methylation profiles of CpG sites associated with age.
Finally, Horvath's epigenetic clock is also the only one that can be applied to several tissues. Indeed, it is the first to accurately measure the epigenetic age of our cells, tissues and/or organs in a distinct and specific waY.
Translated with www.DeepL.com/Translator
Homme/chien, même type d'horloge ?/Man/dog, same type of clock?

L'horloge épigénétique n'est pas réservée aux humains. D'autres espèces subissent également une méthylation de l'ADN avec l'âge, comme les souris, les chimpanzés, les loups et notre meilleur ami : le chien.
Pour savoir en quoi ces horloges diffèrent de la version humaine, le généticien Trey Ideker et son groupe (Université de Californie à San Diego) ont choisi le chien.
Même si les meilleurs amis de l'homme ont divergé par rapport aux humains au début de l'évolution des mammifères, ils constituent en effet un bon groupe de comparaison, car ils vivent dans les mêmes environnements et beaucoup reçoivent des soins de santé et des traitements hospitaliers similaires.
Pour commencer son étude, l'équipe d'Ideker s'est concentrée sur une seule race: les labrador retrievers.
Ils ont analysé les modèles de méthylation de l'ADN dans les génomes de 104 chiens âgés de 4 semaines à 16 ans. Leur analyse a révélé que les chiens et les humains présentaient une méthylation similaire de certaines régions génomiques, liée à l'âge, avec des taux de mutation élevés.
The epigenetic clock is not just for humans. Other species also undergo DNA methylation with age, such as mice, chimpanzees, wolves and our best friend: the dog.
To find out how these clocks differ from the human version, geneticist Trey Ideker and his group (University of California at San Diego) chose the dog.
Although man's best friends diverged from humans at the beginning of mammalian evolution, they are a good comparison group because they live in the same environments and many receive similar health care and hospital treatments.
To begin its study, Ideker's team focused on a single breed: Labrador Retrievers.
They analyzed DNA methylation models in the genomes of 104 dogs aged 4 weeks to 16 years. Their analysis revealed that dogs and humans had similar methylation of certain age-related genomic regions with high mutation rates.
Translated with www.DeepL.com/Translator

Ces similitudes étaient plus évidentes lorsque les scientifiques ont comparé de jeunes chiens et de jeunes humains ou des vieux chiens et des vieillards.
Plus significatif encore, ils ont constaté que certains groupes de gènes impliqués dans le développement sont méthylés de manière similaire au cours du vieillissement chez les deux espèces.
Cela suggère qu'au moins certains aspects du vieillissement ont une origine identique et qu'ils sont conservés de manière évolutive chez les mammifères.
"Nous savions déjà que les chiens souffraient des mêmes maladies et du même déclin fonctionnel du vieillissement que les humains. Ces travaux démontrent que des changements moléculaires similaires se produisent également au cours du vieillissement des deux espèces"
These similarities were more evident when scientists compared young dogs and young humans or old dogs and old people.
More significantly, they found that some groups of genes involved in development are methylated in a similar way during aging in both species.
This suggests that at least some aspects of aging have the same origin and are conserved in an evolutionary manner in mammals.
"We already knew that dogs suffered from the same diseases and functional decline in aging as humans. This work shows that similar molecular changes also occur during the aging of both species"

Âge humain, âge canin : une relation qui n'a rien de linéaire ! Human age, canine age: a relationship that is not linear!

De façon plus anecdotique, ces chercheurs ont proposé une équivalence âge canin/âge humain.
La fameuse relation linéaire (x7) est évidemment fantaisiste. On savait intuitivement que l’horloge épigénétique canine était beaucoup plus rapide, au début, que l’horloge humaine.
A partir de l'étude de la méthylation de l'ADN, ces chercheurs ont établi une courbe logarithmique (la fonction logarithme croit de moins en moins vite).
Pour les labradors ils ont proposé l'équation suivante :
Dog Age = A*ln (Human age) + B
Pour le calcul de la fonction de transfert d'âge, les coefficients A, B ont été estimés à partir de populations égale d'hommes et de chiens. Soit :
Âge Humain d'un chien = 16 ln (âge du chien) + 31
Autant dire qu'à un an, le labrador ne serait plus tout jeune ! En effet ln 1 = 0, il aurait donc déjà 31 ans ! Un handicap insurmontable par rapport à l'humain !
Par contre à 12 ans, le même calcul permettrait de lui attribuer un équivalent âge humain de 71 ans... même pas un senior !
Cette constante fixée à 31 me parait quand même très lourde. Je veux croire que pour mon petit Mélo - le beagle - il y aura un handicap moins sévère. En effet, comme il a 3 ans, ce calcul lui donnerait... 48 ans et 6 mois... alors qu'il court, saute, joue... comme un diable !
La prochaine étape sera donc d'expliquer la durée de vie différente d'une race de chien à une autre... et éventuellement de proposer d'autres équations.
More anecdotally, these researchers proposed a canine age/human age equivalence.
The famous linear relationship (x7) is obviously fanciful. It was intuitively known that the canine epigenetic clock was much faster at first than the human clock.
From the study of DNA methylation, these researchers established a logarithmic curve (the logarithmic function grows less and less quickly).
For the labradors they proposed the following equation:
Dog Age = A*ln (Human age) + B
For the calculation of the age transfer function, the coefficients A, B were estimated from equal populations of men and dogs. Either:
Human Age of a dog = 16 ln (age of the dog) + 31
In other words, by the age of one, the Labrador would no longer be young! Indeed ln 1 = 0, so he would already be 31 years old! An insurmountable handicap compared to humans!
On the other hand, at 12 years old, the same calculation would allow him to be assigned a human age equivalent of 71 years old... not even a senior!
This constant of 31 still seems very heavy to me. I want to believe that for my little Melo - the beagle - there will be a less severe handicap. Indeed, as he is 3 years old, this calculation would give him... 48 years and 6 months... while he runs, jumps, plays... like a devil!
The next step will therefore be to explain the different lifespan of one breed of dog to another... and possibly to propose other equations.

