- AVANT-PROPOS
- A la UNE
- PRESENTATION
- ACTUALITE SCIENTIFIQUE et TECHNOLOGIQUE
- ACTUALITE ARTISTIQUE
- BLOG
- CONSCIENCE
- PLANETE VIVANTE
- SCIENCES
- Sciences et histoire
- Science et politique
- Science/conscience
- Médecine de demain
- Le COVID-19
- COVID-19 - Journal d'une pandémie - 1 -
- COVID-19 - Journal d'une pandémie - 2 -
- COVID-19 - Journal d'une pandémie - 3 -
- COVID-19 - Journal d'une pandémie - 4 -
- COVID-19 - Journal d'une pandémie - 5 -
- COVID-19 - Journal d'une pandémie -6 -
- COVID-19 - Journal d'une pandémie - 7
- COVID-19 - Journal d'une pandémie - 8
- COVID -19 - Journal d'une pandémie - 9
- COVID-19 - Journal d'une pandémie - 10
- COVID-19 - Journal d'une pandemie - 11
- Arts et sciences
- L'homme debout
- Les débuts de la sagesse
- L'épopée scientifique
- Chimie, vivant... une si longue histoire !
- Introduction : 52 choses que je sais d'elle
- Sommaire
- 1 - Premiers pas
- I - A l'origine
- II - De la tetrasomia et l'alchimie à la chimie moderne
- III - al-kimiya
- IV - Alchimie : de l'aube à la fin de la Renaissance
- V - De l'(al)chimie à la chimie : une question de méthode ?
- VI - L'alchimie selon Newton, première partie
- VII - L'alchimie selon Newton, deuxième partie
- 2 - La chimie des Lumières
- XI - Chimie au siècle des Lumières - Introduction
- XII - Chimie au siècle des Lumières- Les affinités électives
- XIII - Diderot et la chimie
- XIV - Diderot - La chimie, pourquoi ?
- XV- Diderot chimiste
- XVI- La chimie et le Rêve de D'Alembert
- 3 - La chimie du vivant
- X - Chimie et Vivant - Introduction
- XIX - La génération spontanée
- XX - Fermentation : duel à 3 !
- XXI - Stéréochimie : clé du Vivant
- XXII - Homochiralité et origine de la vie
- XXIIc - Origine de la vie : état des lieux... provisoire
- XXIIb - Des biopolymères aux premiers organismes vivants
- XXIII- Stéréochimie et activité biologique
- XXIV - Chimie du cerveau - 1- Un cerveau, trois cerveaux, des cerveaux...
- XXV - Chimie du cerveau - 2 - Les neurotransmetteurs, messagers chimiques
- XXVI- Chimie du cerveau -3- Rôle des différents neurotransmetteurs
- XXXIV - Odorat, Odeurs et parfums
- XXXV- Bonnes et mauvaises odeurs
- XXXVI - Chimie et parfums
- XLIII - Chimie et couleur -1- De colore
- XLIV - Chimie et couleur -2- Couleurs végétales
- XLV - Chimie et couleur -3- : chimiothérapie et colorants
- XL- a - ADN, ARN, protéines
- XL- b - Chimie supramoléculaire
- XXXIX- Chimie et Synthetic Biology
- XLVI - Du génome au protéome
- 4 - Chimie et médecine
- VIII - Chimie et médecine : d'Hippocrate à Néron
- IX - Chimie et opium : voyages, voyages !
- XVII- Médecine et Chimie à Montpellier avant la Révolution
- XVIII - Le vitalisme de l'Ecole de Montpellier
- XXIX - Le médicament aujourd'hui
- XXVII - Autour de la sérotonine
- XXVIII - L'ocytocine
- XXX - Chimie, médecine, nanotechnologies
- L - Chimie et dopage -1- La chimie au service du dopage
- LI - Chimie et dopage - 2 - Les outils du chimiste contre le dopage
- XLIX - Image magnétique - 3 - de l'IRM au patient numérique
- 5 - La chimie moderne et ses hommes
- XXXI - Mendeleïev : un tableau de maître !
- XXXII - Mendeleïev : -2- Un chimiste russe au XIXème siècle
- XXXIII - Mendeleïev -3- Le fin mot de l'histoire
- XLI - Paul Sabatier, chimiste languedocien, prix Nobel 1912
- XLII - Victor Grignard, prix Nobel 1912
- XLVII - Image magnétique - 1 - Une histoire de spin
- XLVIII - Image magnétique - 2 - Mais que vient faire le chimiste dans cette galère ?
- 6 - Chimie : bonnes et mauvaises pratiques
- XXXVII- Du mauvais usage de la chimie
- XXXVIII- La chimie passe au vert
- Pour conclure
- Postface - Nylon by DuPont de Nemours
- Nylon... - Part A
- Nylon... - Part B
- Nylon... - Part C
- Nylon... - Part D
- La beauté des mathématiques
- Les sciences vers La Science
- La révolution numérique
- CRISPR-Cas9 : l'édition de gènes
- L'ombre de Frankenstein
- VOIR
- RECHERCHE, CONTACT

Emmanuelle Charpentier et Jennifer Doudna, prix Nobel de Chimie !
Je l'avais annoncé ci-dessous il y a 5 ans :
Magnifique prix Nobel de Chimie pour la Française Emmanuelle Charpentier (avec l'Américaine Jennifer Doudna) et la technique d'édition des gènes CRISPR-Cas 9.
La microbiologiste française, Emmanuelle Charpentier (Max Planck Unit for the Science of Pathogens), est une véritable pionnière dans le domaine. Avec sa consoeur américaine, Jennifer Doudna (Berkeley), elle a montré tout le potentiel du système CRISPR-Cas9 (Cas9 est une endonucléase, permettant de couper l'ADN sur deux zones de coupe actives, une pour chaque brin de la double hélice).
Ce système constitue un extraordinaire tandem pour détecter facilement une séquence d'ADN donnée, puis la découper avec précision.
E. Charpentier a montré qu'il pouvait être utilisé pour supprimer un gène déficient (ou néfaste). Il suffit de fabriquer en laboratoire un « ARN guide » correspondant au gène que l'on souhaite cibler, puis de l'arrimer à une enzyme Cas9.... qui coupe alors ce gène.
Une véritable révolution en génie génétique qui envoie aux oubliettes les méthodes mises au point antérieurement (ZFNs, TALENs).
Leurs principales publications :
- dans Nature,
- dans Science,
- dans Cell.
NB : on ne s'étonnera pas du fait qu'un chercheur de ce calibre, entièrement formé en France, ait été obligé de s'exiler pour trouver les moyens de s'exprimer et d'arriver à ce niveau. Les travaux d'Emmanuelle Charpentier se situaient à l'origine dans le domaine de la recherche fondamentale, délaissée en France par des politiques incompétents (de tous bords), qui ne jurent que par la "recherche appliquée", ignorant que TOUTES les grandes inventions sont issues de la recherche fondamentale.
Crédits faméliques, salaires de misère, administration parfois obtuse, corporatisme, temps perdu sur des appels à projet contrôlés par une petite coterie... la recherche en France traine sa peine et c'est pitié de voir nos meilleurs jeunes s'expatrier.
CRISPR, la percée scientifique de l'année 2015
Révélé, en 2007, par une entreprise spécialisée dans la production de yaourt, identifié comme un mécanisme de défense inconnu utilisé par les bactéries pour combattre les virus, officiellement présenté en 2012, CRISPR, (acronyme pour Clustered Regularly Interspaced Short Palindromic Repeats) est consacré cette année par la revue Science.
A partir de ce mécanisme de défense bactérien, c'est une nouvelle technique de suppression et d'insertion de gènes qui se répand dans les laboratoires, avec en premier lieu l'espoir de traiter de nombreuses maladies génétiques.
La microbiologiste française, Emmanuelle Charpentier (chaire Alexander von Humboldt), est une véritable pionnière dans le domaine. Avec sa consoeur américaine, Jennifer Doudna (Berkeley), elle a montré tout le potentiel du système CRISPR-Cas9 (Cas9 est une endonucléase, permettant de couper l'ADN sur deux zones de coupe actives, une pour chaque brin de la double hélice).
Ce système constitue un extraordinaire tandem pour détecter facilement une séquence d'ADN donnée, puis la découper avec précision.
E. Charpentier a montré qu'il pouvait être utilisé pour supprimer un gène déficient (ou néfaste). Il suffit de fabriquer en laboratoire un « ARN guide » correspondant au gène que l'on souhaite cibler, puis de l'arrimer à une enzyme Cas9.... qui coupe alors ce gène.
Une véritable révolution en génie génétique qui envoie aux oubliettes les méthodes mises au point antérieurement (ZFNs, TALENs).
L'américaine Jennifer Doudna et la française Emmanuelle Charpentier, futurs prix Nobel ?
CRISPR everywhere
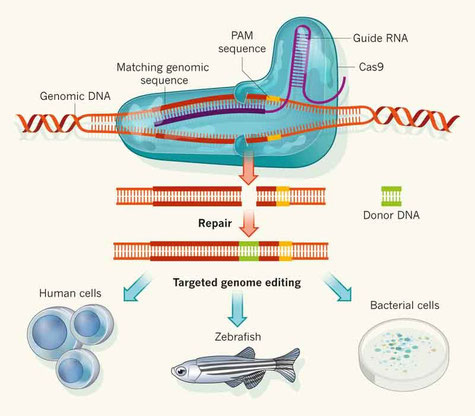
"Pour le meilleur ou pour le pire, CRISPR-cas9 transforme la biologie. Nous sommes maintenant à l'aube de l'âge de l'édition de gènes."
"Researchers the world over have rushed to use the tool to tinker with the genomes of human somatic cells, viruses, bacteria, animals and plants, and it's in these contexts that the technique promises to have more immediate impact."
Le point dans Nature sur cette fantastique technique qui révolutionne la biologie.
Mars 2016


Jennifer Doudna (UC Berkeley / HHMI): Genome Engineering with CRISPR-Cas9
CRISPR : maintenant on découpe aussi l'ARN
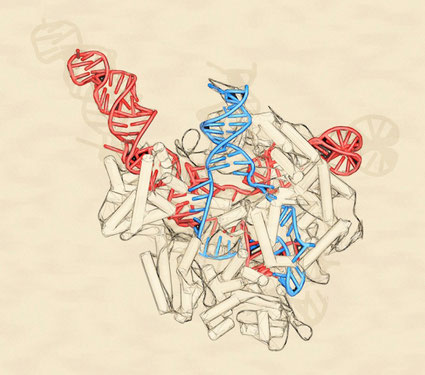
Deux méthodes ont été développées à cet effet par deux pionniers de CRISPR-Cas9 :
- Jennifer Doudna, à Berkeley
- Feng Zhang, (Broad Institute of MIT and Harvard)
L'une sur les cellules de mammifères, l'autre sur des bactéries.
Vu le nombre considérable de publications mensuelles sur le sujet, il ne s'agit que d'un modeste début !
Edition des gènes, CRISPR : le problème éthique

Une équipe chinoise franchit le Rubicon
Lors du deuxième Sommet international sur la modification du génome humain, qui réunissait à Hong Kong, cette semaine, les scientifiques concernés, les débats ont été surtout alimentés par l'annonce de l'équipe de He Jiankui (chercheur en édition du génome à l'Université chinoise des sciences et technologies de Shenzhen) selon laquelle il aurait imprégné une femme d'embryons modifiés pour les rendre résistants à l'infection à VIH.
Dans une vidéo diffusée sur YouTube, ce chercheur, indique que cette femme aurait donné naissance à des jumelles en bonne santé,
Notons que ce résultat n'a pas encore donné lieu à publication dans une revue à comité de lecture.
Cette annonce a aussitôt provoqué une tempête dans la communauté scientifique.
L'indignation des chercheurs concernés est générale (y compris dans l'université concernée).
Ils mettent en doute le bien-fondé d’une procédure préliminaire potentiellement dangereuse, sans consensus scientifique international.
Aujourd'hui, certains pensent également que cette annonce pourrait avoir un effet dissuasif sur l'édition de gènes.
En 2015 déjà, des chercheurs chinois avaient annoncé dans la revue Nature, avoir modifié génétiquement des embryons humains.

26 février 2019
Il n’existe toujours pas de preuve définitive que le biophysicien ait effectivement réussi à modifier les gènes des filles - ou ceux d’un troisième enfant qui devrait naître plus tard cette année.
Cependant l'affaire fait grand bruit dans le monde scientifique.
En introduisant des mutations dans des embryons humains, qui ont ensuite été utilisés pour produire des bébés, il est entré de manière insidieuse dans une ère où la science pouvait réécrire le pool génétique de l'homme en modifiant la lignée germinale humaine. Il a également bafoué les normes établies en matière de sécurité et de protection humaine.
Aujourd'hui, He Jiankui a été limogé de son université et la police chinoise enquête.
Vie synthétique vs édition de gènes
La fulgurante ascension de la technique d'édition de gènes CRISPR-Cas9, dont je parle abondamment par ailleurs, relègue-t'elle au second plan les recherches des groupes de San Diego (voir sur le site les travaux de Floyd Romesberg et Craig Venter) qui visent à créer ex nihilo des organismes synthétiques, ou semi-synthétiques, destinés à produire médicaments, carburants et bien d'autres molécules ?
En d'autres termes à quoi bon faire compliqué en fabriquant une nouvelle forme de vie, quand il devient si facile de modifier l'existant ?
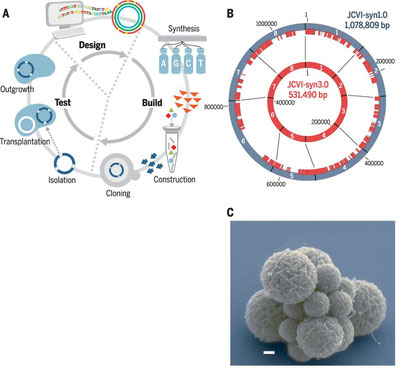
Craig Venter continue néanmoins sa route à marche forcée ; son équipe vient de décrire la synthèse d'une bactérie possédant le plus petit génome existant- JCVI-syn3.0 - (531 paires de bases pour 473 gènes). Son temps de doublement - 180 minutes - est tout à fait respectable.
Ce génome est plus petit que celui de la cellule minimale se répliquant de façon autonome dans la nature.
Cependant sur la voie de la minimisation du génome, beaucoup de chemin reste à parcourir pour trouver le bon compromis entre la taille du génome et le taux de croissance.
Jusqu'ici le groupe de Venter a plutôt fonctionné par tâtonnement, sur le mode essais/erreurs et de nombreux points d'interrogations subsistent. Il a ainsi observé que 149 gènes (près du tiers) de ce génome avaient des fonctions biologiques inconnus, mais étaient indispensables. Pourquoi ?
En fait, ces deux approches du travail sur le vivant se situent sur deux plans différents.
Avec CRISPR, c'est un bricolage -génial- permettant la réparation de l'existant qui se développe et va donner des résultats spectaculaires très rapidement.
Les travaux sur la vie synthétique sont plus ambitieux, puisqu'ils visent avant tout à élucider le mécanisme de la vie et sa reproduction a minima. Ils se situent bien en amont et leurs applications ne se dessineront qu'à moyen terme.
Craig Venter, comme tous les pionniers de la biologie synthétique aime à rappeler cette phrase de Richard Feynman :
« Ce que je ne peux pas créer, je ne le comprends pas "